국내 증시의 전반적인 하락세에서도 메지온이 남다른 주가 흐름을 보여주고 있다. 지난해 11월 3만원대였던 주가가 8만원을 훌쩍 넘어섰다. 폰탄수술 치료제 글로벌 임상 3상의 주요 결과 발표시점이 가까워졌고, 판매 승인 이후에도 기대할 만한 동력들이 있다는 분석이다.
1일 메지온에 따르면 이 회사는 신약후보물질 유데나필을 이용해 미국 캐나다 한국 등에서 임상 3상을 진행 중이다. 지난 6월 400명 규모의 환자 모집을 완료했다. 약 6개월의 추적관찰 기간을 감안하면 연내 임상시험이 마무리되고, 내년 1분기에는 주요 결과가 공개될 것으로 보고 있다.

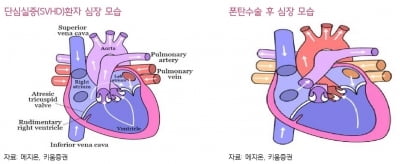
폰탄수술은 선천성 심장기형 중 하나인 단심실 환자들에게 시행하는 수술이다. 그러나 20세가 넘어가면 호흡 기능이 급속도로 떨어지면서 만성심부전증 간경화 간암 등 여러 합병증으로 환자 대부분이 사망에 이르게 된다. 유데나필은 앞선 임상에서 경쟁 물질 대비 심각한 부작용 없이, 심장 기능 및 운동능력을 향상시켰다.
폰탄수술 치료제 환자수도 예상보다 많은 점도 긍정적이다. 메지온은 기존에 미국의 폰탄수술 환자수를 약 3만명으로 추정했다. 그러나 최근 개최된 2018 바이오 인베스터 포럼에서 진단코드를 조회해본 결과, 예상되는 폰탄수술 환자수가 7만7966명으로 2배 이상이었다.
여기에 판매허가를 받게 되면 우선심사권(PRV)도 획득하게 된다. PRV는 열대성 및 희귀질환 신약개발을 촉진하기 위해 미 식품의약국(FDA)가 만든 제도다. 신약 승인 검토기간을 6개월로 단축해 준다. 다른 기업에게 판매도 가능하다.
정승규 키움증권 연구원은 "현재까지 23개의 신약에 대해 PRV가 발급됐으며, 평균 거래금액은 약 1700억원 수준"이라며 "메지온 역시 희귀질환인 폰탄수술 치료제를 개발하고 있기 때문에 메지온의 기업가치를 산정할 때 PRV 가치를 감안하는 것이 합리적"이라고 말했다.
한민수 한경닷컴 기자 hms@hankyung.com
누리바이오 "췌장암, 폐암 진단 키트로 미국 시장 먼저 진출...
"대형 바이오시밀러·임상 후기 바이오텍 선호"-현대차
바이오協·충주시, 바이오헬스케어 산업 육성 MOU